何が変わったか
これまで iPS 細胞から作る免疫療法用 T 細胞は、(1) がんを直接攻撃する「キラー T 細胞 (CD8+)」が研究の中心で、(2) 免疫の司令塔役を担う「ヘルパー T 細胞 (CD4+)」の分化誘導は技術的に難しく、(3) 数少ない誘導成功例も「フィーダー細胞 (足場細胞)」としてマウス由来細胞を使う必要があり、ヒトへの臨床応用には規制上のハードルが残っていた。
京都大学 iPS 細胞研究所 (CiRA) の研究グループが Molecular Therapy 誌 (doi:10.1016/j.ymthe.2026.01.020) に発表した研究は、Notch シグナルと TCR シグナルの「段階別調整」によりフィーダー細胞を一切使わずヒト iPS 細胞から CD4 単陽性ヘルパー T 細胞を誘導することに成功し、得られた細胞はキラー T 細胞を上回る量のサイトカインを分泌、さらに自身でがん細胞を攻撃する能力までを獲得することを示した。
社会にどんな影響があるか
主たる影響として、抗がん剤治療で「免疫疲弊」を起こした患者にも適用可能な次世代の iPS 由来がん免疫療法の臨床応用ハードルが大きく下がる。フィーダー細胞依存はマウス由来細胞・ウシ血清等の使用を伴い、GMP (医薬品製造管理基準) 準拠の製造ラインで規制対応コストが高かった。今回のフィーダーフリー手法は「規制的にクリーンな細胞」を作れるため、CAR-T 療法等の次世代展開で量産・輸送・凍結保存などの工業化ハードルも同時に下がる。
一方で副作用として、ヘルパー T 細胞は強力なサイトカイン分泌能を持つため、輸注後のサイトカイン放出症候群 (CRS) リスクは既存の CAR-T 療法より高くなる可能性がある。研究段階では in vitro / 動物モデルレベルの結果であり、ヒト試験での免疫過剰反応制御は次の課題として残る。
ニュースの詳細
研究グループは先行研究でマウスフィーダー細胞由来の人工胸腺オルガノイド上で CD4+ T 細胞の誘導に成功していたが、今回はそのシグナル伝達経路を分子レベルで解析し、Notch シグナルと TCR シグナルを「分化段階に応じて精密に制御する」手法を確立。これによりフィーダー細胞を完全に除いた条件で CD4+ ヘルパー T 細胞の誘導に到達した。
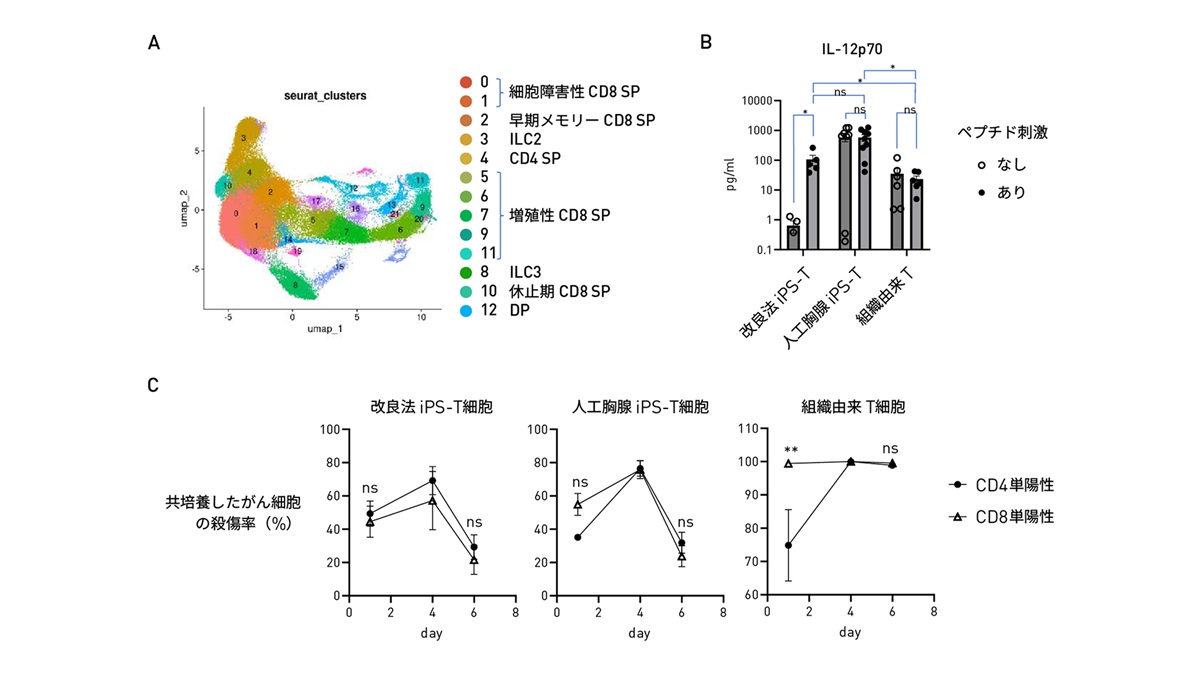
得られた CD4+ T 細胞は、(1) 高い増殖能力、(2) 免疫反応活性化分子 ThPOK・CD40L の高発現、(3) キラー T 細胞を上回るサイトカイン分泌量、(4) がん細胞認識による樹状細胞の成熟誘導 (= 免疫起点の構築)、(5) 増殖過程での自発的ながん細胞傷害活性 (キラー T 細胞同等以上の殺傷率) を備えていることが確認された。論文は Molecular Therapy 誌 (Cell Press 系) に掲載され、京都大学リサーチニュースは2026年4月24日にプレスリリースを公開。大学ジャーナルが5月3日に解説記事として配信した。