何が変わったか
これまでアルツハイマー病の記憶障害については、海馬の神経細胞死やアミロイドβ沈着が主たる原因として研究の焦点であり、神経伝達物質ドーパミンの関与は限定的に扱われてきた。
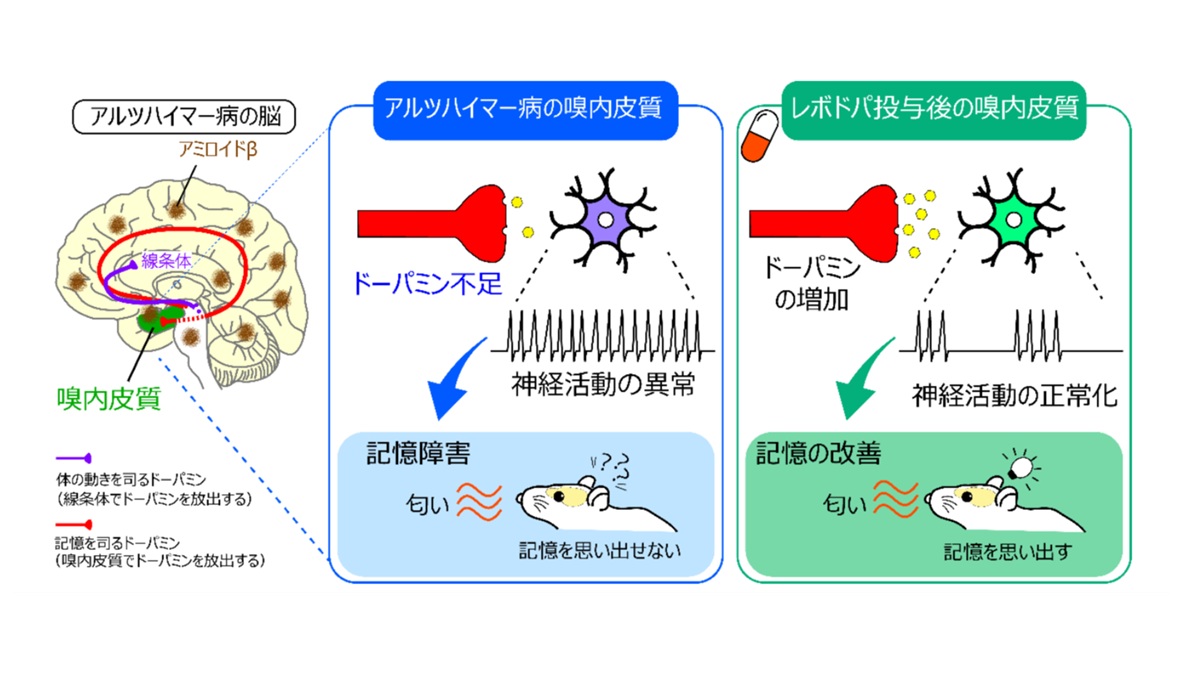
東北大学大学院とカリフォルニア大学アーバイン校の国際共同研究チームは、アルツハイマー病マウスを用い、海馬のすぐ隣にある「嗅内皮質」のドーパミン量が健常マウスの 5 分の 1 以下まで減少しており、これが記憶障害を引き起こしていることを発見した。さらに、嗅内皮質のドーパミンを増やす治療実験を行うと、アルツハイマー病マウスは再び匂いを記憶できた。
社会にどんな影響があるか
主たる影響として、パーキンソン病治療薬「レボドパ」を投与してもアルツハイマー病マウスの嗅内皮質神経活動が正常に近づき記憶が改善したことから、既存薬の応用というローコストな新治療法開発の道筋が開ける。新規分子の創製は通常 10 年単位の時間と多額の投資を要するが、既存薬のリポジショニング (適応拡大) は安全性試験を相当部分省略できる。
副作用として、マウスでの結果がヒトでどこまで再現するかという翻訳研究の障壁が常に残る。アルツハイマー病患者の脳でもドーパミン働きの低下は示唆されているが、嗅内皮質の役割と治療応答性については詳細な臨床研究が必要。
ニュースの詳細
研究チームは 2021 年に嗅内皮質の神経細胞がドーパミンを受け取ることで記憶が形成されることを発見しており、今回はこの神経細胞の機能低下がアルツハイマー病の記憶障害を生む可能性を検証した。アルツハイマー病マウスは匂いを覚えられない特徴を持ち、匂いを嗅いでいるときの嗅内皮質ドーパミン量を測定したところ健常マウスの 5 分の 1 以下となり、神経細胞が覚えるべき匂いに正しく応答できなくなる異常も観察された。
キーワード解説
嗅内皮質 (entorhinal cortex) とは、海馬の隣接領域で、感覚情報を海馬に送り込む「入口」として機能する大脳皮質領域。記憶形成・空間認知に重要で、アルツハイマー病で最も早期に病変が現れる領域の一つとして知られる。
レボドパ (L-DOPA, Levodopa) とは、パーキンソン病の標準的治療薬。脳内でドーパミンに変換される前駆体で、血液脳関門を通過する性質を活かし、不足したドーパミンを補う。今回のアルツハイマー研究で記憶改善効果が示されたことで、リポジショニングの可能性が浮上した。
ノックインモデル とは、特定の遺伝子に変異を導入したマウスなどの遺伝子改変動物。アルツハイマー病研究ではアミロイドβ前駆体タンパク質 (APP) など患者で変異が見つかる遺伝子をマウスに同型導入することで、ヒトの病態に近いモデルを作製する。